魔立方 网站建设线上推广方式
PART 01
接地通孔应位于接地参考层开关处
流经所布线路的所有电流都有相等的回流。耦合策略固然很多,不过回流通常流经相邻的接地层或与信号线路并行布置的接地。在参考层继续时,所有耦合都仅限于传输线路,一切都非常正常。不过,如果信号线路从顶层切换至内部或底层时,回流也必须获得路径。
图1就是一个实例。顶层信号线路电流下面紧挨着就是回流。当它转移到底层时,回流就通过附近的通孔。不过,如果附近没有用于回流的通孔时,回流就要通过最近可用的接地通孔。
更远的距离会产生电流环路,形成电感器。如果这种不必要的电流路径偏移,碰巧又同另一条线路交叉,那么干扰就会更严重。这种电流环路其实相当于形成了一个天线!

图1:信号电流从器件引脚经过通孔流到较低层。回流在被迫流向最近通孔改变至不同参考层之前位于信号之下。唯样商城自建高效智能仓储,拥有自营库存超100,000种,提供一站式正品现货采购、个性化解决方案、选型替代等多元 化服务。
接地参考是最佳策略,但高速线路有时候可布置在内部层上。接地参考层上下都放置非常困难,半导体厂商可能会受到引脚限制,把电源线安放在高速线路旁边。参考电流要是需要在非DC耦合的各层或各网之间切换,应紧挨着开关点安放去耦电容。
PART 0 2 将器件焊盘与顶层接地连接起来
许多器件在器件封装底部都采用散热接地焊盘。在RF器件上,这些通常都是电气接地,而相邻焊盘点有接地通孔阵列。可将器件焊盘直接连接至接地引脚,并通过顶层接地连接至任何灌铜。如有多个路径,回流会按路径阻抗比例拆分。通过焊盘进行接地连接相对于引脚接地而言,路径更短、阻抗更低。
电路板与器件焊盘之间良好的电气连接至关重要。装配时,电路板通孔阵列中的未填充通孔也可能会抽走器件的焊膏,留下空隙。填满通孔是保证焊接到位的好办法。
在评测中,还要打开焊接掩模层确认没有焊接掩模在器件下方的电路板接地上,因为焊接掩模可能会抬高器件或使其摇摆。
PART 03
无参考层间隙
器件周边到处都是通孔。 电源网分解成本地去耦,然后降至电源层,通常提供多个通孔以最大限度减少电感,提高载流容量,同时控制总线可降至内层。 所有这些分解最终都会在器件附近完全被钳住。
每个这些通孔都会在内接地层上产生大于通孔直径自身的禁入区,提供制造空隙。这些禁入区很容易在回流路径上造成中断。一些通孔彼此靠近则会形成接地层沟,顶层CAD视图看不见,这将导致情况进一步复杂化。
图2两个电源层通孔的接地层空隙可产生重叠的禁入区,并在返回路径上造成中断。回流只能转道绕过接地层禁入区,形成现在常见的发射感应路径问题。

图2:通孔周围接地层的禁入区可能重叠,迫使回流远离信号路径。即便没有重叠,禁入区也会在接地层形成鼠咬阻抗中断
甚至“友好型”接地通孔也会为相关金属焊盘带来电路板制造工艺要求的最小尺寸规格。通孔如果非常靠近信号线路,就会产生好像顶层接地空隙被老鼠咬掉一块一样的侵蚀。图2是鼠咬示意图。
由于禁入区由CAD软件自动生成,通孔在系统电路板上的使用又很频繁,因此先期布局过程几乎总会出现一些返回路径中断问题。
布局评测时要跟踪每条高速线路,检查相关回流层以避免中断。让所有可在任何区域产生接地层干扰的通孔更靠近顶层接地空隙是一个不错的方法。
PART 0 4 保持差分线路的差 分性
回流路径对信号线路性能至关重要,其应视为信号路径的一部分。与此同时,差分对通常没有紧密耦合,回流可能流经相邻层。两个回流必须通过相等的电气路径布线。
即便在差分对的两条线路不紧密耦合时,邻近与共享型设计限制也会让回流处于相同层。要真正保持低寄生信号,需要更好的匹配。差分组件下接地层的断流器等任何计划结构都应是对称的。
同样,长度是否匹配可能也会产生信号线路中的波形曲线问题。回流不会引起波形曲线问题。一条差分线路的长度匹配情况应在其它差分线路中体现。
PART 0 5 RF信号线路附近没有时钟或控制线路
时钟和控制线路有时可视为没什么影响的邻居,因为其工作速度低,甚至接近DC。不过,其开关特性几乎接近方波,可在奇数谐波频率下生成独特的音调。
方波发射能源的基本频率虽然不会产生什么影响,但其锐利的边缘可能会有影响。在数字系统设计中,转折频率可估算必须要考虑的最高频率谐波,计算方式为:Fknee=0.5/Tr,这里的Tr是上升时间。
请注意,是上升时间,而不是信号频率。不过锐利边缘的方波也有强大的高阶奇数谐波,其可能只在错误频率下下降并耦合在RF线路上,违反严格的传输掩模要求。
时钟和控制线路应由内部接地层或顶层接地灌流(ground pour)与RF信号线路隔离。如果不能使用接地隔离信号,那么线路布线应确保直角交叉。因为时钟或控制线路发射的磁通线路会围绕干扰源线路的电流形成放射柱形等高线,它们将不会在接收器线路中产生电流。
放慢上升时间不但可降低转折频率,而且还有助于减少干扰源的干扰,但时钟或控制线路也可充当接收器线路。接收器线路仍可作为将寄生信号导入器件的导管。
PART 0 6 使用接地隔离高速线路
微波传输带与带线大多数都与相邻接地层耦合。一些通量线路仍沿水平方向散发,并端接于相邻迹线。一条高速线路或差分对上的音调在下一条迹线上终结,但信号层上的接地灌流会为通量线路带来较低阻抗的终点,让邻近迹线不受音调干扰。
时钟分布或合成器设备路由出来、用于承载相同频率的迹线集群可能相邻而行,因为干扰源音调已经存在于接收器线路上。不过,分组的线路最终会分散。
分散时,应在分散线路之间提供接地灌流,并在其开始分散的地方灌入通孔,以便感应回流沿着额定回流路径流回。在图3中,接地岛末端的通孔可使感应电流流到参考层上。接地灌流上其它通孔之间的间隔不要超过一个波长的十分之一,以确保接地不会成为共振结构。
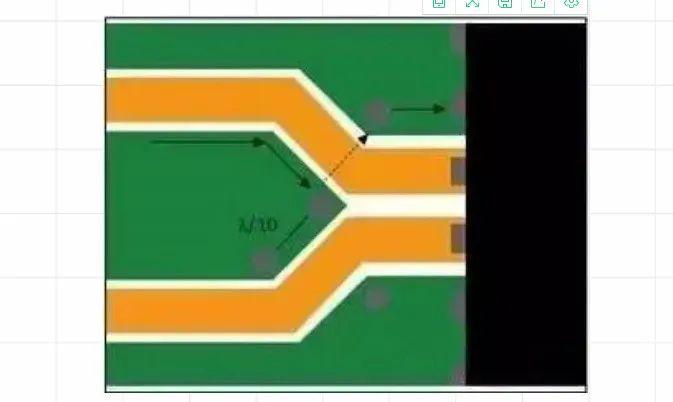
图3:差分线路分散处的顶层接地通孔为回流提供流动路径
PART 0 7 不要在噪声较大的电源层进行RF线路布线
音调进入电源层就会扩散到每个地方。如果杂散音调进入电源、缓冲器、混频器、衰减器和振荡器,就会对干扰频率进行调制。
同样,当电源到达电路板时,它还没有彻底被清空而实现对RF电路系统的驱动。应最大限度减少RF线路在电源层的暴露,特别是未过滤的电源层。
邻近接地的大型电源层可创建高质量嵌入式电容,使寄生信号衰减,并用于数字通信系统与某些RF系统。另一种方法是使用最小化电源层,有时更像是肥大迹线而不能说是层,这样RF线路更容易彻底避开电源层。
这两种方法都可行,不过决不能将二者的最差特性凑在一起,也就是既使用小型电源层,又在顶部走线RF线路。
PART 0 8 让去耦靠近器件
去耦不仅有助于避免杂散噪声进入器件,还可帮助消除器件内部生成的音调,避免其耦合到电源层上。去耦电容越靠近工作电路系统,效率就越高。本地去耦受电路板迹线的寄生阻抗干扰较小,较短的迹线支持较小的天线,减少有害音调发射。
电容器安放要结合最高自共振频率,通常最小值、最小外壳尺寸、最靠近器件,以及越大的电容器,离器件越远。在RF频率下,电路板背面的电容器会产生通孔串连接地路径的寄生电感,损失大量噪声衰减优势。
PART 0 9 简单总结
通过电路板布局评测,我们可发现可能发射或接收杂散RF音调的结构。要跟踪每一条线路,有意识地明确其回流路径,确保它能够与线路并行,特别是要彻底检查过渡。
此外,还要将潜在干扰源与接收器隔离。按照一些简单直观的规则降低寄生信号,可加速产品发布,降低调试成本。
